2019年高考化学试卷(天津)(解析卷)
2019年天津市高考化学试卷解析版参考答案与试题解析一、选择题(共6小题,每小题6分,满分36分)1.(6分)化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是( )A.利用废弃的秸秆生产生物质燃料乙醇B.利用石油生产塑料、化纤等高分子材料C.利用基本的化学原料生产化学合成药物D.利用反渗透膜从海水中分离出淡水【考点】18:物理变化与化学变化的区别与联系.菁优网版权所有【分析】A.秸秆通过发酵生成乙醇;B.石油生产塑料、化纤,裂化生成小分子,小分子发生加聚反应生成高分子;C.基本的化学原料生产化学合成药物,发生有机反应生成新物质;D.利用反渗透膜从海水中分离出淡水,无新物质生成。【...
相关推荐
-
小学生交通安全常识VIP免费

 2024-12-01 8
2024-12-01 8 -
小学生公共场所礼仪VIP免费

 2024-12-01 8
2024-12-01 8 -
小学生歌曲优美歌词摘抄VIP免费

 2024-12-01 8
2024-12-01 8 -
小学生必看的十部电影VIP免费

 2024-12-01 12
2024-12-01 12 -
小学生安全用电知识VIP免费

 2024-12-01 13
2024-12-01 13 -
小学教师精彩课堂教学用语教师言语道德集锦VIP免费

 2024-12-01 31
2024-12-01 31 -
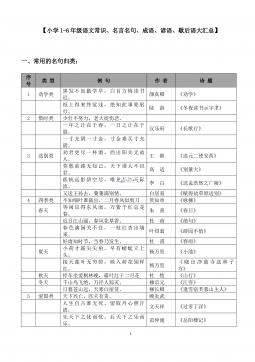
小学1-6年级语文常识、名言名句、成语、谚语、歇后语大汇总VIP免费
 2024-12-01 25
2024-12-01 25 -
五年级奥数期末测试卷VIP免费

 2024-12-01 31
2024-12-01 31 -
六年级计算题的复习与回顾练习VIP免费

 2024-12-01 12
2024-12-01 12 -
小学生礼仪常识VIP免费

 2024-12-01 22
2024-12-01 22
相关内容
-

小学二年级上册上学期-部编版语文:寒号鸟 预习笔记
分类:幼儿/小学教育
时间:2025-08-25
标签:无
格式:PDF
价格:10 玖币
-

小学二年级上册上学期-部编版语文:古诗二首预习笔记
分类:幼儿/小学教育
时间:2025-08-25
标签:无
格式:PDF
价格:10 玖币
-

小学二年级上册上学期-部编版语文:第一课时预习笔记
分类:幼儿/小学教育
时间:2025-08-25
标签:无
格式:PDF
价格:10 玖币
-

小学二年级上册上学期-部编版语文:第三课时预习笔记
分类:幼儿/小学教育
时间:2025-08-25
标签:无
格式:PDF
价格:10 玖币
-

小学二年级上册上学期-部编版语文:第二课时预习笔记
分类:幼儿/小学教育
时间:2025-08-25
标签:无
格式:PDF
价格:10 玖币




 渝公网安备50010702506394
渝公网安备50010702506394
