专题16 物质结构与性质综合题-五年(2019-2023)高考化学真题分项汇编(全国通用)(解析版)
五年(2019-2023)年高考真题分项汇编专题16物质结构与性质综合题〖2023年高考真题〗1.(2023·全国甲卷)将酞菁—钴钛—三氯化铝复合嵌接在碳纳米管上,制得一种高效催化还原二氧化碳的催化剂。回答下列问题:(1)图1所示的几种碳单质,它们互为_______,其中属于原子晶体的是_______,间的作用力是_______。(2)酞菁和钴酞菁的分子结构如图2所示。酞菁分子中所有原子共平面,其中轨道能提供一对电子的原子是_______(填图2酞菁中原子的标号)。钴酞菁分子中,钴离子的化合价为_______,氮原子提供孤对电子与钴离子形成_______键。(3)气态通常以二聚体的形式存在,其...
相关推荐
-
政治理论应知应会 100 题VIP免费

 2024-12-12 394
2024-12-12 394 -
2025年中央机关及其直属机构录用公务员考试 行政职业能力测验(地市级)(经典模考卷三)解析VIP免费

 2024-12-12 48
2024-12-12 48 -
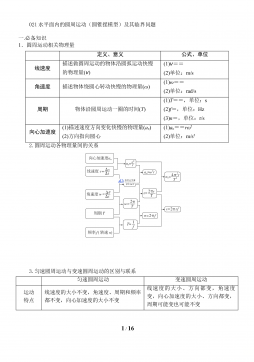
021水平面内的圆周运动(圆锥摆模型)及其临界问题 精讲精练-2022届高三物理一轮复习疑难突破微专题VIP免费
 2025-01-04 48
2025-01-04 48 -
21学位英语:从句考点真题VIP免费

 2025-04-08 7
2025-04-08 7 -
19学位英语:2010年阅读理解分析VIP免费

 2025-04-08 4
2025-04-08 4 -
[16] 学位英语:2007年阅读理解分析VIP免费

 2025-04-08 5
2025-04-08 5 -
[15] 学位英语:2006年阅读理解分析VIP免费

 2025-04-08 11
2025-04-08 11 -
[14] 学位英语:2005年阅读理解分析VIP免费

 2025-04-08 13
2025-04-08 13 -
[13] 学位英语:2004年阅读理解分析VIP免费

 2025-04-08 10
2025-04-08 10 -
[10] 学位英语:长难句拆分(二)VIP免费

 2025-04-08 11
2025-04-08 11
相关内容
-

[16] 学位英语:2007年阅读理解分析
分类:高等教育
时间:2025-04-08
标签:无
格式:DOC
价格:5.9 玖币
-

[15] 学位英语:2006年阅读理解分析
分类:高等教育
时间:2025-04-08
标签:无
格式:DOC
价格:5.9 玖币
-

[14] 学位英语:2005年阅读理解分析
分类:高等教育
时间:2025-04-08
标签:无
格式:DOC
价格:5.9 玖币
-

[13] 学位英语:2004年阅读理解分析
分类:高等教育
时间:2025-04-08
标签:无
格式:DOC
价格:5.9 玖币
-

[10] 学位英语:长难句拆分(二)
分类:高等教育
时间:2025-04-08
标签:无
格式:DOC
价格:5.9 玖币




 渝公网安备50010702506394
渝公网安备50010702506394
