2019年高考化学试卷(新课标Ⅲ)(解析卷)
2019年全国统一高考化学试卷(新课标Ⅲ)参考答案与试题解析一、选择题:本题共7个小题,每小题6分。共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。1.(6分)化学与生活密切相关。下列叙述错误的是( )A.高纯硅可用于制作光感电池B.铝合金大量用于高铁建设C.活性炭具有除异味和杀菌作用D.碘酒可用于皮肤外用消毒【分析】A.Si为半导体材料,能作电池;B.铝合金大量用于高铁建设;C.活性炭具有吸附性;D.碘酒能使蛋白质变性。【解答】解:A.Si为半导体材料,能作光感电池,故A正确;B.铝合金在生活中用途最广泛,大量用于高铁建设,故B正确;C.活性炭具有吸附性,没有强氧化性,所以活...
相关推荐
-
2021 年全国硕士研究生入学统一考试英语(一)试题及参考答案VIP免费

 2024-12-02 4
2024-12-02 4 -
2016年一级注册消防工程师消防安全案例分析VIP免费

 2024-12-03 7
2024-12-03 7 -
2017年注册消防工程师案例分析真题解析VIP免费

 2024-12-03 4
2024-12-03 4 -
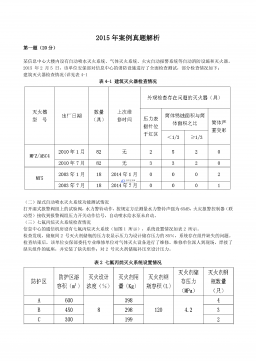
2015年注册消防工程师案例真题解析VIP免费
 2024-12-03 35
2024-12-03 35 -
2019年注册消防工程师案例分析真题解析VIP免费

 2024-12-03 39
2024-12-03 39 -
消防综合能力真题按章节版(2015-2019年)VIP免费

 2024-12-03 16
2024-12-03 16 -
消防技术实务真题按章节版(2015-2019)VIP免费

 2024-12-03 15
2024-12-03 15 -
2018年注册消防工程师案例分析真题解析VIP免费

 2024-12-03 28
2024-12-03 28 -
2006年中央、国家机关公务员录用考试行政职业能力测试真题及答案解析(A类)【完整+答案+解析】VIP免费

 2024-12-13 121
2024-12-13 121 -
2008年0706河南公务员考试《行测》真题VIP免费

 2025-02-25 14
2025-02-25 14
相关内容
-

2007年天津市公务员考试《行测》真题(春季卷)答案及解析
分类:
时间:2025-02-07
标签:无
格式:PDF
价格:5.9 玖币
-

2005年江苏省公务员考试《行测》真题(B类卷)答案及解析
分类:
时间:2025-02-07
标签:无
格式:PDF
价格:5.9 玖币
-

2010年广东公务员考试《行测》真题(部分题目缺失)
分类:
时间:2025-02-25
标签:无
格式:PDF
价格:5.9 玖币
-

2010年北京公务员考试《行测》真题
分类:
时间:2025-02-25
标签:无
格式:PDF
价格:5.9 玖币
-

2008年0706河南公务员考试《行测》真题
分类:
时间:2025-02-25
标签:无
格式:PDF
价格:5.9 玖币




 渝公网安备50010702506394
渝公网安备50010702506394
