2024版 化学新教材鲁科版(闽粤皖京豫)教师用书配套课件第6章化学反应与能量转化第6章 第34讲 化学反应的热效应
VIP免费
2024-11-17
5
0
3.91MB
16 页
5.9玖币
侵权投诉
第34 讲 化学反应的热效应
[复习目标] 1.了解反应热、内能、焓变的概念,知道化学反应热效应与内能和反应的焓变
之间的关系。2.知道常见的吸热反应和放热反应,能从多角度分析化学反应中能量变化的原
因。3.了解热化学方程式的含义,能正确书写热化学方程式。4.了解摩尔燃烧焓的概念及能
源利用的意义。
考点一 反应热 焓变
1.体系与环境
(1)体系:人为划定的研究对象 ( 物质系统 ) 。
(2)环境:体系以外的其他部分。
2.反应热与内能
(1)反应热(Q):当化学反应在一定的温度下进行时,反应所释放或吸收的热量称为该反应在
此温度下的热效应。
(2)内能
3.反应热与焓变
4.吸热反应、放热反应
(1)放热反应:释放热量的化学反应。反应物的总能量大于反应产物的总能量。反应体系的
能量降低,故 ΔH<0,即 ΔH为负值。
(2)吸热反应:吸收热量的化学反应。反应物的总能量小于反应产物的总能量。反应体系的
能量升高,故 ΔH>0,即 ΔH为正值。
(3)常见的吸热反应和放热反应
吸热反应(ΔH>0) 放热反应(ΔH<0)
①Ba(OH)2·8H2O与NH4Cl 的反应
② 大多数的分解反应
③ 弱电解质的电离
④ 盐类水解
⑤C和H2O(g)、C和CO2的反应
① 中和反应
② 燃烧反应
③ 金属与酸或与氧气的反应
④ 铝热反应
⑤ 酸性氧化物或碱性氧化物与水的反应
⑥ 大多数的化合反应
5.反应热产生的原因
(1)从能量图分析
(2)从化学键变化分析
1.浓H2SO4稀释是放热反应( )
2.放热反应不需要加热就能发生,吸热反应不加热就不能发生( )
3.石墨转变为金刚石是吸热反应,则金刚石比石墨更稳定( )
4.可逆反应的 ΔH表示完全反应时的热量变化,与反应是否可逆无关( )
5.吸热反应中,反应物化学键断裂吸收的总能量高于反应产物形成化学键放出的总能量
( )
6.活化能越大,表明化学反应吸收的能量越多( )
答案 1.× 2.× 3.× 4.√ 5.√ 6.×
一、对反应过程能量图的理解
1.科学家用 X射线激光技术观察到 CO 与O在催化剂表面形成化学键的过程。反应过程的
示意图如图。
回答下列问题:
(1)从状态Ⅰ到状态Ⅲ为________(填“吸热”或“放热”)反应。
(2)从状态Ⅰ到状态Ⅱ需要________(填“吸收”或“释放”)能量,CO 分子________(填
“是”或“否”)需要断键形成 C和O。
(3)从状态Ⅱ到状态Ⅲ形成的化学键是____________________________________________。
(4)将相同物质的量的 CO 转化为 CO2,CO 与O比CO 与O2反应放出的热量________(填
“多”或“少”),可能的原因是___________________________________________________
___。
(5)由该反应过程可知,在化学反应中,旧化学键________(填“一定”或“不一定”)完全断
裂,但一定有新化学键的________。
答案 (1)放热 (2)吸收 否 (3)碳氧双键(或C==O) (4)多 CO 与O2反应生成 CO2需要先
吸收能量断裂 O2分子中的共价键 (5)不一定 形成
2.臭氧层中 O3分解过程如图所示,回答下列问题。
(1)ΔH________(填“>”或“<”)0。
(2)催化反应①是________(填“吸热”或“放热”,下同)反应,催化反应②是________反应。
(3)总反应的活化能是________,催化反应①的活化能是________,催化反应②对应的逆反
应的活化能是______,总反应对应的逆反应活化能为________。
答案 (1)< (2)吸热 放热 (3)E E1 E2+|ΔH| E+|ΔH|
3.铋基催化剂对 CO2电化学还原制取 HCOOH 具有高效的选择性。其反应历程与能量变化
如图所示,其中吸附在催化剂表面上的物种用*标注。
CO2――→CO――→HCOO-――→HCOOH
(1)使用 Bi、Bi2O3两种催化剂哪个更有利于 CO2的吸附?________。简述判断依据:______
______________________________________________________________________。
(2)CO2电化学还原制取 HCOOH 反应的 ΔH________(填“>”或“<”)0。
(3)使用 Bi 催化剂时,最大能垒是____________,使用 Bi2O3催化剂时,最大能垒是_______
______________________________________________________________________。
(4)由*CO 生成*HCOO-的反应为_________________________________________________。
答案 (1)Bi2O3 由题图可知,使用 Bi2O3催化剂时,相对能量减小得多,趋于更稳定状态
(2)<
(3)0.38 eV 0.32 eV (4)*CO+HCO+e-===*CO+*HCOO-
解析 (3)使用 Bi 催化剂时,*CO2―→*CO 过程中的活化能最大,为-0.51 eV-(-0.89 eV)
=0.38 eV,使用 Bi2O3催化剂时,*CO―→*CO+*HCOO-过程的活化能最大,为-2.54 eV-
(-2.86 eV)=0.32 eV。
二、根据键能计算焓变
4.CH3—CH3(g)―→CH2==CH2(g)+H2(g) ΔH,有关化学键的键能如下表:
化学键 C—H C==C C—C H—H
键能/(kJ·mol-1)414 615 347 435
则该反应的反应热为____________。
答案 +125 kJ·mol-1
解析 ΔH=E(C—C)+6E(C—H)-E(C==C)-4E(C—H)-E(H—H)=(347+6×414-615-
4×414-435) kJ·mol-1=+125 kJ·mol-1。
5.已知几种化学键的键能数据如下表所示(亚硝酰氯的结构式为 Cl—N==O):
化学键 N≡OCl—Cl Cl—N N==O
键能/(kJ·mol-1)630 243 a607
则反应 2NO(g)+Cl2(g)2ClNO(g)的ΔH=________kJ·mol-1(用含 a的代数式表示)。
答案 289-2a
解析 根据 ΔH=反应物总键能-生成物总键能知,ΔH=2×630 kJ·mol-1+243 kJ·mol-1-
2×(a kJ·mol-1+607 kJ·mol-1)=(289-2a) kJ·mol-1。
熟记常见 1 mol 下列物质中化学键数目:
物质 金刚石 SiO2P4CO2CH4
化学键 C—C Si—O P—P C==O C—H
化学键数目 2NA4NA6NA2NA4NA
摘要:
展开>>
收起<<
第34讲 化学反应的热效应[复习目标] 1.了解反应热、内能、焓变的概念,知道化学反应热效应与内能和反应的焓变之间的关系。2.知道常见的吸热反应和放热反应,能从多角度分析化学反应中能量变化的原因。3....
声明:本站为文档C2C交易模式,即用户上传的文档直接被用户下载,本站只是中间服务平台,本站所有文档下载所得的收益归上传人(含作者)所有。玖贝云文库仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对上载内容本身不做任何修改或编辑。若文档所含内容侵犯了您的版权或隐私,请立即通知玖贝云文库,我们立即给予删除!
相关推荐
-
曲一线系列初中《5中考3年模拟》2023专题解释全国道德与法治资料包05专题五 走进社会生活 遵守社会规则VIP免费

 2024-11-21 24
2024-11-21 24 -
曲一线系列初中《5中考3年模拟》2023专题解释全国道德与法治资料包05专题五 走进社会生活 遵守社会规则VIP免费

 2024-11-21 21
2024-11-21 21 -
曲一线系列初中《5中考3年模拟》2023专题解释全国道德与法治资料包03专题三 青春时光 做情绪情感的主人VIP免费

 2024-11-21 15
2024-11-21 15 -
曲一线系列初中《5中考3年模拟》2023专题解释全国道德与法治资料包03专题三 青春时光 做情绪情感的主人VIP免费

 2024-11-21 19
2024-11-21 19 -
曲一线系列初中《5中考3年模拟》2023专题解释全国道德与法治资料包02专题二 友谊的天空 师长情谊VIP免费

 2024-11-21 19
2024-11-21 19 -
曲一线系列初中《5中考3年模拟》2023专题解释全国道德与法治资料包02专题二 友谊的天空 师长情谊VIP免费

 2024-11-21 20
2024-11-21 20 -
曲一线系列初中《5中考3年模拟》2023专题解释全国道德与法治资料包01专题一 成长的节拍 生命的思考VIP免费

 2024-11-21 21
2024-11-21 21 -
曲一线系列初中《5中考3年模拟》2023专题解释全国道德与法治资料包01专题一 成长的节拍 生命的思考VIP免费

 2024-11-21 21
2024-11-21 21 -
曲一线系列初中《5中考3年模拟》2023专题解释全国道德与法治资料包《53中考》全国道德与法治资料包VIP免费

 2024-11-21 24
2024-11-21 24 -
曲一线系列初中《5中考3年模拟》2023专题解释全国道德与法治资料包07专题七 坚持宪法至上 崇尚法治精神VIP免费

 2024-11-21 18
2024-11-21 18
分类:中学教育
价格:5.9玖币
属性:16 页
大小:3.91MB
格式:DOCX
时间:2024-11-17
作者详情
相关内容
-

2025届重庆市西南大学附属中学高三下学期5月全镇模拟物理试题(含答案)
分类:中学教育
时间:2025-12-31
标签:无
格式:PDF
价格:10 玖币
-

2025届重庆市西南大学附属中学高三下学期5月全镇模拟化学试题(含答案)
分类:中学教育
时间:2025-12-31
标签:无
格式:PDF
价格:10 玖币
-
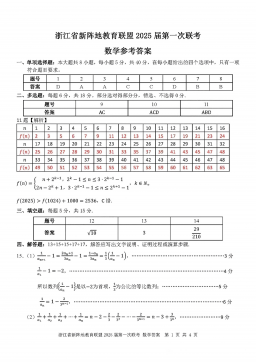
2025届浙江省新阵地联盟高三10月联考数学答案
分类:中学教育
时间:2025-12-31
标签:无
格式:PDF
价格:10 玖币
-

2025届重庆市西南大学附属中学高三下学期5月全镇模拟数学试题(含答案)
分类:中学教育
时间:2025-12-31
标签:无
格式:PDF
价格:10 玖币
-

2025届重庆康德三诊英语+答案
分类:中学教育
时间:2026-01-03
标签:无
格式:PDF
价格:10 玖币




 渝公网安备50010702506394
渝公网安备50010702506394
