2010年高考化学试卷(山东)(解析卷)
2010年山东省高考化学试卷参考答案与试题解析 一、选择题(共7小题,每小题4分,满分28分)1.(4分)(2010•山东)16O和18O是氧元素的两种核素,NA表示阿伏加德罗常数,下列 说法正确的是()A.16O2与18O2互为同分异构体B.16O2与18O2核外电子排布方式不同C.通过化学变化可以实现16O与18O间的相互转化D.标准状况下,1.12L 16O2和1.12L 18O2均含0.1NA个氧原子【考点】同位素及其应用.菁优网版权所有【分析】本题考查了同位素、原子核外电子排布、阿伏加德罗常数等知识点.【解答】解:A、16O2与18O2是同一种物质,都是氧气,故A错; B、两...
相关推荐
-
政治理论应知应会 100 题VIP免费

 2024-12-12 394
2024-12-12 394 -
2025年中央机关及其直属机构录用公务员考试 行政职业能力测验(地市级)(经典模考卷三)解析VIP免费

 2024-12-12 48
2024-12-12 48 -
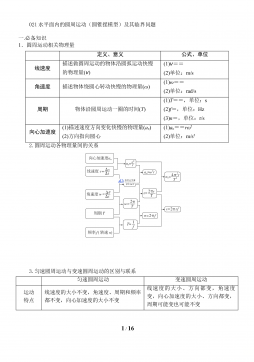
021水平面内的圆周运动(圆锥摆模型)及其临界问题 精讲精练-2022届高三物理一轮复习疑难突破微专题VIP免费
 2025-01-04 48
2025-01-04 48 -
21学位英语:从句考点真题VIP免费

 2025-04-08 7
2025-04-08 7 -
19学位英语:2010年阅读理解分析VIP免费

 2025-04-08 4
2025-04-08 4 -
[16] 学位英语:2007年阅读理解分析VIP免费

 2025-04-08 5
2025-04-08 5 -
[15] 学位英语:2006年阅读理解分析VIP免费

 2025-04-08 11
2025-04-08 11 -
[14] 学位英语:2005年阅读理解分析VIP免费

 2025-04-08 13
2025-04-08 13 -
[13] 学位英语:2004年阅读理解分析VIP免费

 2025-04-08 10
2025-04-08 10 -
[10] 学位英语:长难句拆分(二)VIP免费

 2025-04-08 11
2025-04-08 11
相关内容
-

[16] 学位英语:2007年阅读理解分析
分类:高等教育
时间:2025-04-08
标签:无
格式:DOC
价格:5.9 玖币
-

[15] 学位英语:2006年阅读理解分析
分类:高等教育
时间:2025-04-08
标签:无
格式:DOC
价格:5.9 玖币
-

[14] 学位英语:2005年阅读理解分析
分类:高等教育
时间:2025-04-08
标签:无
格式:DOC
价格:5.9 玖币
-

[13] 学位英语:2004年阅读理解分析
分类:高等教育
时间:2025-04-08
标签:无
格式:DOC
价格:5.9 玖币
-

[10] 学位英语:长难句拆分(二)
分类:高等教育
时间:2025-04-08
标签:无
格式:DOC
价格:5.9 玖币




 渝公网安备50010702506394
渝公网安备50010702506394
